-
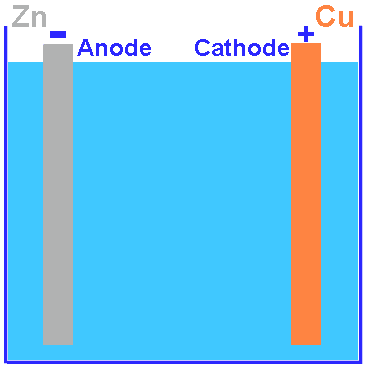
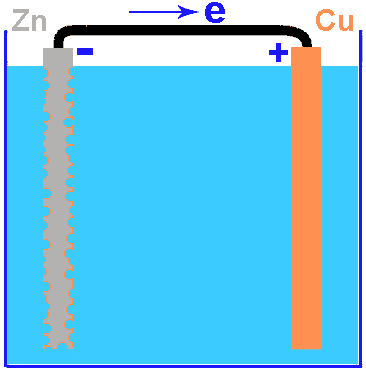
Inleiding: batterijen en electronegativiteit van metalenVoordat ik het over galvanische bescherming voor schepen heb, moet ik het eerst over batterijen hebben. De eerste batterij was de zuil van Volta, bestaande uit een stapel kleine zink- en koperen schijven, gescheiden door vilt geïmpregneerd met een zoutoplossing. Alle moderne batterijen zijn gebaseerd op dit principe: twee verschillende metalen en een elektrolyt.Wanneer de batterij stroom levert (het elektrische circuit is gesloten), oxideren de zinkschijven en lossen ze langzaam op in de elektrolyt. Wanneer de batterij geen stroom levert, voorkomt de negatieve lading die op de elektrode verschijnt oxidatie. Wanneer het circuit gesloten is, kan de lading via de geleider wegvloeien en kan de oxidatie opnieuw beginnen. De twee diagrammen rechts geven niet exact een Voltaïsche batterij weer (het is in werkelijkheid een stapel elementen), maar de componenten zijn hetzelfde. Het verschil tussen een normale batterij en een oplaadbare batterij is dat de reactie bij een oplaadbare batterij omkeerbaar is. Bij een normale batterij is opladen niet mogelijk omdat het geoxideerde zink in de oplossing terechtkomt en bij reductie niet goed op de elektrode neerslaat, maar dendrieten vormt die de batterij kortsluiten (de batterij van Volta heeft nog andere nadelen die we hier niet zullen bespreken). Deze oxidatiereactie kan echter ook in andere gevallen optreden: hiervoor zijn nodig:
Magnesium Mangaan Aluminium Zink Chroom IJzer Koper Nikkel Zilver Tin Kwik Platina Goud Koolstof Omdat meer elektronegatieve metalen niet worden aangetast, worden ze "edele" metalen genoemd. Bij de ijzer-zinkverbinding wordt het zink aangetast, maar bij de ijzer-nikkelverbinding wordt het ijzer aangetast. Het aangetaste ijzer verandert in roest (ijzeroxide). Het probleem met ijzer is dat de oxidelaag enorm groeit en loslaat van het ijzer, waardoor een nieuwe laag bloot komt te liggen. Bij de oxidatie van aluminium, chroom en andere metalen vormt zich een oxidelaag die niet groeit. Deze laag blijft aan het metaal vastzitten en beschermt het tegen oxidatie. Daarom dat een laagje nikkel op staal het staal beschermt: nikkel oxideert, maar de oxidelaag is ondoordringbaar en beschemt het onderliggend metaal.
Bescherming van scheepsrompenScheepsrompen zijn over het algemeen van staal gemaakt. Maar staal is samengesteld uit ijzer, koolstof en andere legeringsmetalen (we beschouwen koolstof als een metaal vanwege één van zijn eigenschappen: het is geleidend).We hebben dus alle elementen om een batterij te maken, namelijk twee verschillende metalen in contact met elkaar, ondergedompeld in een elektrolyt (zeewater of brak water). Zonder een beschermingssysteem zou de romp snel corroderen. Het is hier niet mogelijk om een potentiaalverschil te meten, omdat het ijzer en de koolstof in het staal gemengd zijn. In een batterij met een ijzeren elektrode en een koolstofelektrode ontstaat een potentiaalverschil, waarbij de ijzeren elektrode negatiever is (dit is de anode), die corrodeert tijdens het ontladen van de batterij. Een klassieke saline batterij heeft een positieve koolstofpool (dit is de kleine elektrode in het midden) terwijl de negatieve electrode de buitenste zinklaag is. Tijdens het ontladen van de batterij corrodeert het zink. De batterij kan gemakkelijk gaan lekken wanneer er geen zink meer in metaalvorm aanwezig is. Zink-koolstofbatterijen worden hier uitgelegd. Het eenvoudigste systeem, toegepast in kleine schepen en polyester schepen zoals de oudere mijnenjagers van de Aster-klasse (Eridan in Frankrijk), maakt gebruik van zinkblokken rond de meest corrosiegevoelige delen (aan de achtersteven). Op mijnenjagers beschermen deze blokken de bronzen schroef, die praktisch het enige ondergedompelde metalen onderdeel is. Voor een goede werking moeten de zinkblokken verbonden zijn met de aarding van het schip (elektrische aarding) en met alle onderdelen die gevoelig zijn voor corrosie (de schroefas in het geval van mijnenjagers). Als de elektrische verbinding tussen de zinkblokken en de aarding van het schip verbroken is, kan een klein potentiaalverschil worden gemeten en werkt de cathodische bescherming niet meer. Deze zinkblokken corroderen en verdwijnen uiteindelijk. Tijdens het droogdokonderhoud worden ze vervangen. Deze zinkblokken worden ook wel opofferingsanodes genoemd, omdat ze zichzelf in feite opofferen om de andere metalen onderdelen van het schip te beschermen.
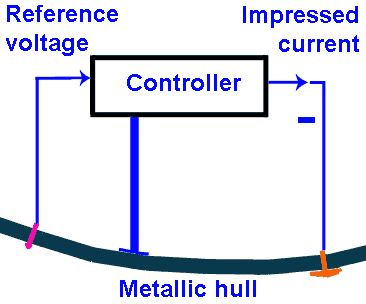
Actieve beschermingVoor grote schepen zijn opofferingsanodes niet langer voldoende, zeker niet als het schip veel heeft gevaren en de verflaag niet meer in goede staat verkeert. Er zouden zoveel anodes nodig zijn dat het systeem onpraktisch zou worden.Maar wat produceren opofferingsanodes? Ze produceren een potentiaalverschil (en dus een stroom, omdat het elektrische circuit gesloten is) dat het staal beschermt. In actieve systemen wordt dit potentiaalverschil gecreëerd met behulp van elektroden die zijn aangesloten op een stroombron. Deze elektroden zijn gemaakt van platina, bedekt met een dunne laag iridium. De elektroden corroderen niet, hoewel ze dezelfde functie vervullen als de zinkblokken. De elektroden zijn actief, niet vanwege hun reactiviteit (het zijn edele metalen), maar vanwege de negatieve spanning die erop wordt aangelegd. Omdat water een goede geleider is, moet er een stroom van enkele ampères door de elektroden lopen, zelfs als de spanning erg laag is. In bepaalde zeer specifieke gevallen worden zinkblokken nog steeds gebruikt, zelfs als het schip een actief beschermingssysteem heeft. Bijvoorbeeld bij schepen in aanbouw of tijdens onderhoud, wanneer het actieve beschermingssysteem niet kan worden gebruikt (geen stroomvoorziening). In dat geval wordt een metalen nets met zinkblokken te water gelaten, dat elektrisch is verbonden met de scheepsromp. Op grote schepen maakt het actieve beschermingssysteem (Impressed Current Cathodic Protection, of ICCP) het schip zeer zichtbaar voor onderwatermijnen, die het potentiaalverschil kunnen detecteren. Bovendien produceert de draaiende schroef een zeer karakteristieke rimpeling in het elektrische veld, waardoor zelfs het scheepstype kan worden geïdentificeerd. De beschermingsstroom moet daarom tot een minimum worden beperkt, mede omdat een te hoge stroom waterstof op de kathode (stalen romp) produceert. Deze waterstofafgifte kan het staal na verloop van tijd broos maken. Het schip kan dus onvoldoende beschermd zijn (het zal roesten) of overbeschermd, wat ook slecht is voor de romp. De optimale stroom wordt bepaald door een tweede elektrode die het potentiaal van het staal ten opzichte van het water meet. De meetelektrode is gemaakt van zilver en produceert een zeer stabiele referentiespanning ten opzichte van het water, waardoor de spanning van het staal ten opzichte van het water eenvoudig kan worden bepaald door aftrekking. De correcte werking van de referentie-elektrode kan worden vastgesteld door vergelijking met de spanning van andere referentie-elektroden als het schip meerdere beveiligingssystemen heeft. Er kan ook een draagbare referentie-elektrode worden gebruikt, die in water wordt ondergedompeld in de buurt van de te testen referentie-elektrode. Alle metingen worden uitgevoerd ten opzichte van de massa van het schip. Grote schepen hebben meerdere ICCP-systemen aan boord, elk bestaande uit een stroomgenerator, één of meer beschermingsanodes en een referentie-elektrode. Dit beschermingssysteem is niet beperkt tot militaire schepen, maar is van toepassing op alle schepen met een metalen romp. |
Publicités - Reklame
 Er is verwarring tussen electropositiviteit en electronegativiteit. Eigenlijk mogen we enkel van electronegativiteit spreken: een metaal is niet "meer electropositief" maar "minder electronegatief". Deze tabel toont enkele elementen met hun electronegativiteit: natrium, magnesium, aluminium,...
Er is verwarring tussen electropositiviteit en electronegativiteit. Eigenlijk mogen we enkel van electronegativiteit spreken: een metaal is niet "meer electropositief" maar "minder electronegatief". Deze tabel toont enkele elementen met hun electronegativiteit: natrium, magnesium, aluminium,...